北京內容評審官
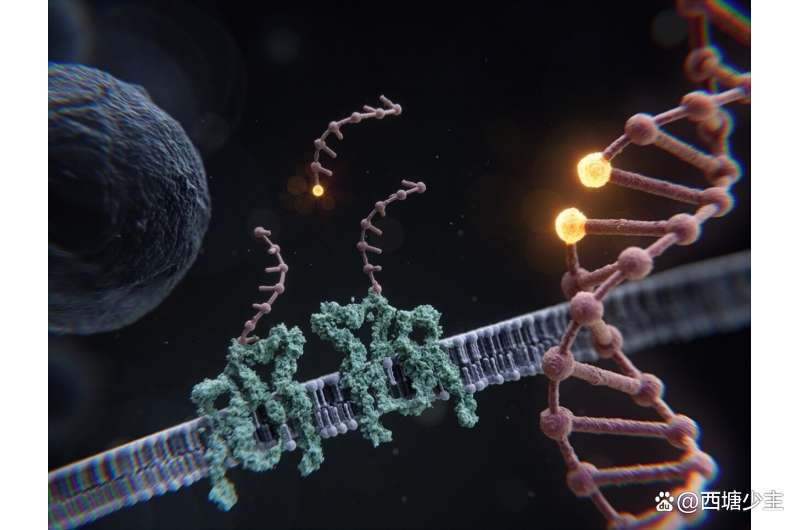
RESI能夠以?ngstr?m分辨率跨長度尺度進行顯微鏡觀察:從單個蛋白質的整個細胞到DNA中兩個相鄰堿基之間的距離。學分:馬克斯·伊格萊西亞斯
馬克斯普朗克生物化學研究所(MPIB)和慕尼黑路德維希-馬克西米利安大學(LMU)的Ralf Jungmann研究小組在熒光顯微鏡方面取得了突破。該團隊開發了順序成像分辨率增強(RESI),這是一項革命性的技術,可將熒光顯微鏡的分辨率提高到?ngstr?m級。這項創新有望為我們研究生物系統的方法帶來范式轉變,迄今為止沒有的細節。
細胞是生命的基本單位,包含大量維持和延續生命系統的復雜結構、過程和機制。許多細胞核心成分,如DNA、RNA、蛋白質和脂質,只有幾納米的大小。這使得它們大大小于傳統光學顯微鏡的分辨率J限。因此,這些分子和結構的確切組成和排列通常是未知的,導致對生物學基本方面缺乏機械理解。
近年來,超分辨率技術在分辨光的經典衍射J限以下的許多亞細胞結構方面取得了突飛猛進的進步。單分子定位顯微鏡(SMLM)是一種超分辨率方法,可以通過暫時分離其單個熒光發射來解析十納米大小的結構。
當單個目標在其他黑暗的視野中隨機點亮(它們閃爍)時,它們的位置可以用亞衍射精度確定。由Jungmann小組發明的DNA-PAINT是一種SMLM技術,它使用染料標記的DNA“成像器”鏈與其靶標結合補體的瞬時雜交,以實現超分辨率所需的閃爍。然而,迄今為止,即使是DNA-PAINT也無法解析*小的細胞結構。
在目前發表在《自然》雜志上的研究中,由共同**作者Susanne Reinhardt,Luciano Masullo,Isabelle Baudrexel和Philipp Steen以及Jungmann領導,該團隊在超分辨率顯微鏡中引入了一種新方法,該方法從根本上實現了“無限”的空間分辨率。
這項新技術稱為通過順序成像增強分辨率,簡稱RESI,利用DNA-PAINT通過獨特的DNA序列編碼目標身份的能力。通過標記相鄰的靶標,即使通過超分辨率顯微鏡也無法分辨,使用不同的DNA鏈,將額外的分化程度(條形碼)引入樣品中。通過對**個序列進行順序成像,然后對另一個序列(從而對目標序列)進行成像,現在可以明確地分離它們。
至關重要的是,當它們按順序成像時,目標可以任意接近彼此,這是其他技術無法解決的問題。此外,RESI不需要專門的儀器,事實上,它可以使用任何標準的熒光顯微鏡進行應用,使幾乎所有研究人員都可以輕松使用。
為了證明RESI在分辨率上的飛躍,該團隊為自己設定了解決生物系統中*小空間距離之一的挑戰:沿著DNA雙螺旋的單個堿基之間的分離,間隔不到一納米。
通過設計DNA折紙納米結構,使其呈現單鏈DNA序列,這些序列從一個堿基對距離從雙螺旋突出,然后依次對這些單鏈進行成像,研究小組解決了相鄰堿基之間0.85納米(或8.5 ?ngstr?m)的距離,這是以前無法想象的壯舉。研究人員以1 ?ngstr?m或10億分之一米的精度完成了這些測量,強調了RESI方法沒有的功能。
重要的是,該技術是通用的,不**于DNA納米結構的應用。為此,研究小組研究了利妥昔單抗的分子作用模式,利妥昔單抗是一種抗CD20單克隆抗體,于1997年首次被批準用于治療CD20陽性血癌。然而,研究這些藥物分子對分子受體模式的影響已經超出了傳統顯微鏡技術的空間分辨率能力。了解這些模式是否以及如何在健康和疾病以及治療中發生變化,不僅對基本機制研究很重要,而且對設計新的靶向疾病療法也很重要。
使用RESI,Jungmann和他的團隊能夠揭示未處理細胞中CD20受體作為二聚體的自然排列,并揭示CD20如何在藥物治療后重新排列成二聚體鏈。單蛋白水平的見解現在有助于闡明利妥昔單抗的分子作用模式。
由于RESI是在完整的完整細胞中進行的,因此該技術縮小了純結構技術(如X射線晶體學或低溫電子顯微鏡)與傳統的低分辨率全細胞成像方法之間的差距。Jungmann和他的團隊堅信,“這種沒有的技術不僅對超分辨率,而且對整個生物學研究都是真正的游戲規則改變者。
更多信息:Susanne C. M. Reinhardt 等人,?ngstr?m 分辨率熒光顯微鏡,《自然》(2023 年)。DOI: 10.1038/s41586-023-05925-9
期刊信息:自然
原文章鏈接:https://baijiahao.baidu.com/s?id=1766916376197887830&wfr=spider&for=pc
文章來源于網絡,如果有侵權,請聯系我們刪除,謝謝~

